致命眼癌在人体细胞和活体动物中的扩散得到遏制
11/12/2018
约翰·霍普金斯大学医学院对存在/不存在癌症扩散的眼癌儿童进行了研究,通过比较儿童的基因序列,研究人员在报告中提供了新证据,证明细胞中的多米诺骨牌效应是导致癌症扩散的原因。他们通过实验成功地在斑马鱼和人类细胞中找到事件链的阻断部分——该部分让眼癌细胞停止生长和扩散。
研究人员表示,这项新发现使治疗儿童最常见眼癌视网膜母细胞瘤前景喜人。世界卫生组织的数据显示,这种癌症估计每年影响7000~8000人,全球每年死于该病的儿童数量多达 4000人。
该实验报告于 11月6日发表在《Oncogene》期刊上。
约翰·霍普金斯大学医学院病理学系的研究助理教授Laura Asnaghi博士说:“扩散性视网膜母细胞瘤缺乏有效的治疗方法。但是如果在肿瘤扩散之前能及时发现,我们就有机会治疗这种致命癌症。因此,我们研究了肿瘤侵袭的原因,这可以帮助我们开发靶向治疗以防止这种侵袭。”
为了揭示肿瘤扩散相关的一系列分子作用,约翰斯·霍普金斯大学的研究人员首先分析了10名不同患者的组织,其中5名患有侵袭性肿瘤,5名患者患有非侵袭性肿瘤。他们比较了这两组肿瘤的RNA谱,发现与非侵袭性细胞相比,在侵袭性视网膜母细胞瘤细胞中,编码激活素A受体1C型(ACVR1C)的基因的RNA水平增加了2到3倍。这一发现非常重要,因为目前医学界已知道激活素受体基因在其它癌症中的作用,包括胆囊癌和乳腺癌。研究人员认为,激活素受体可能是抑制视网膜母细胞瘤癌症扩散和生长的关键靶点。
通常而言,当激活素受体检测到生长信号时,就会触发细胞生长和分裂。研究人员使用一种名为SB505124的药物处理细胞,阻断活化素受体检测其它生长信号,来观察会发生什么。他们将药物和细胞放在过滤器上,通过观察过滤器的细胞数量来测量侵袭情况。结果显示,用药物处理后的视网膜母细胞瘤细胞,在生长、增殖和侵袭方面的抑制程度达到 60%至80%。
确认了激活素受体在扩散型视网膜母细胞瘤细胞中的作用后,研究人员进一步希望了解其是否适用于活体动物。接下来的实验在斑马鱼胚胎中进行,因为其胚胎尚未完全发展免疫系统,并且不会排斥移植其中的其他类型细胞。人视网膜母细胞瘤细胞被注射到两天大的斑马鱼眼中,随后在接下来的4~6天内测量眼肿瘤的直径,监测癌细胞的生长和扩散。
然后,相同的药物SB505124被用来抑制斑马鱼眼睛的激活素。研究人员表示,与未注射该药物的斑马鱼眼相比,用药后的眼部肿瘤的直径减小了55%。Asnaghi说,总体而言,实验显示阻断激活素受体可以有效抑制侵袭性视网膜母细胞瘤细胞在体内的生长和扩散。
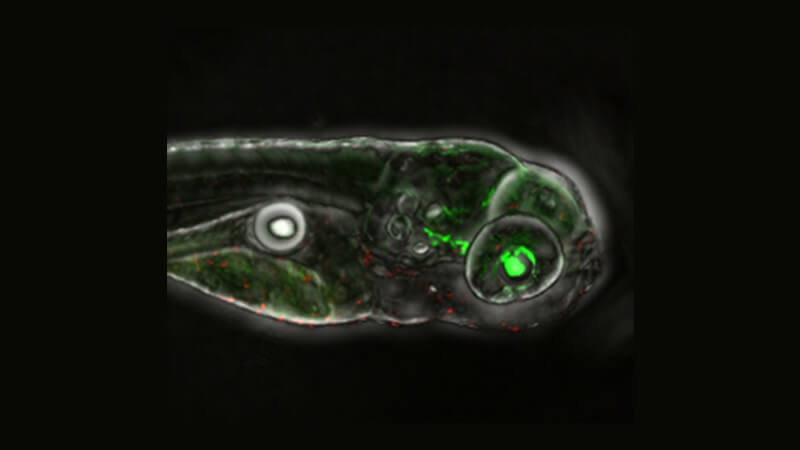
用药物处理后的视网膜母细胞瘤细胞成批死亡 (见图中红色部分)
Asnaghi表示: “我们希望这项研究结果为视网膜母细胞瘤提供新的治疗方法,在美国和全世界范围内为更多受视网膜母细胞瘤影响的儿童提供视力保护并改善预后状况。但目前我们只能持有谨慎乐观态度,还需要更多研究才能安全地为患者开发或测试相关疗法。”
